医疗器械经营综合许可办事指南
医疗器械经营综合许可操作手册
一、办理依据
《医疗器械监督管理条例》
《医疗器械经营监督管理办法》
二、本地特色改革文件
《平顶山市人民政府办公室关于在全市医疗器械经营行业推行综合许可改革的意见(试行)》(平政办〔2022〕21号)
《平顶山市市场监督管理局关于印发<平顶山市医疗器械经营综合许可改革实施办法(试行)>的通知》(平市监〔2022〕55号)
三、受理单位
平顶山市市场监督管理局
四、材料清单

(扫码查看具体内容)
五、材料模板

(扫码查看具体内容)
六、业务事项
医疗器械经营综合许可申请类型: □新办 □变更 □延续
包含子项
主营项目(必选):
第三类经营许可 □新办 □变更 □延续 □合并 □补发 □注销
兼营项目(至少选择一项):
第二类经营备案 □新办 □变更 □合并 □补发 □取消
网络销售备案 □备案 □合并 □取消
第一类生产备案 □新办 □变更 □合并 □补发 □取消
第一类产品备案 □新办 □变更 □合并 □补发 □取消
七、办理方式
1.网上办理:通过“河南政务服务网”-选择“河南省-平顶山市-市场监督管理局”点击对应业务进行在线办理。
2.窗口办理:医疗器械综合许可业务可以一窗通办。
窗口地址:河南省平顶山市新华区兴平路与清风路交叉口西80米平顶山市政务大数据中心5楼 A59、 A60综合受理窗口。
八、办结时限
1.法定办结时限:20个工作日
2.承诺办结时限:
涉及现场检查的为10个工作日(涉及限期整改的,整改时间不包含在内);
不涉及现场检查的为1个工作日。
九、办理结果
《医疗器械经营综合许可证》
十、收费情况
本业务不涉及收费。
十一、综合受理流程图

(扫码查看具体内容)
十二、咨询电话
0375-2692076、0375-2580030、0375-2588113
十三、投诉电话
0375-2692260、0375-2588128
医疗器械经营综合许可办事指南
附材料清单库与材料模板!
可下载、可编辑!
证 样

基本信息
1、设立依据
《医疗器械监督管理条例》
《医疗器械经营监督管理办法》
《平顶山市人民政府办公室关于在全市医疗器械经营行业推行综合许可改革的意见(试行)》
《平顶山市医疗器械经营综合许可改革实施办法(试行)》等
2、办证机关
平顶山市市场监督管理局
3、办理时限
涉及现场检查的为10个工作日(涉及限期整改的,整改时间不包含在内);
不涉及现场检查的为1个工作日。
4、项目内容
主营项目(必选):
第三类医疗器械经营
兼营项目(可选择一种或者多种):
第二类医疗器械经营
医疗器械网络销售
第一类医疗器械生产备案
第一类医疗器械产品备案
重大利好!“办三送二”!
即在申请综合许可证的时候,主营项目选择“第三类医疗器械经营”、兼营项目选择“第二类医疗器械经营”的,免于提交证明符合第二类医疗器械经营条件的材料。只需提交证明符合第三类医疗器械经营条件的材料,最后核发一张综合许可证,包含《医疗器械经营许可证》和《第二类医疗器械经营备案凭证》的信息。
通俗来讲,相当于办理第三类医疗器械经营许可证的同时,附送第二类医疗器械经营备案凭证!
01流程图(示例)
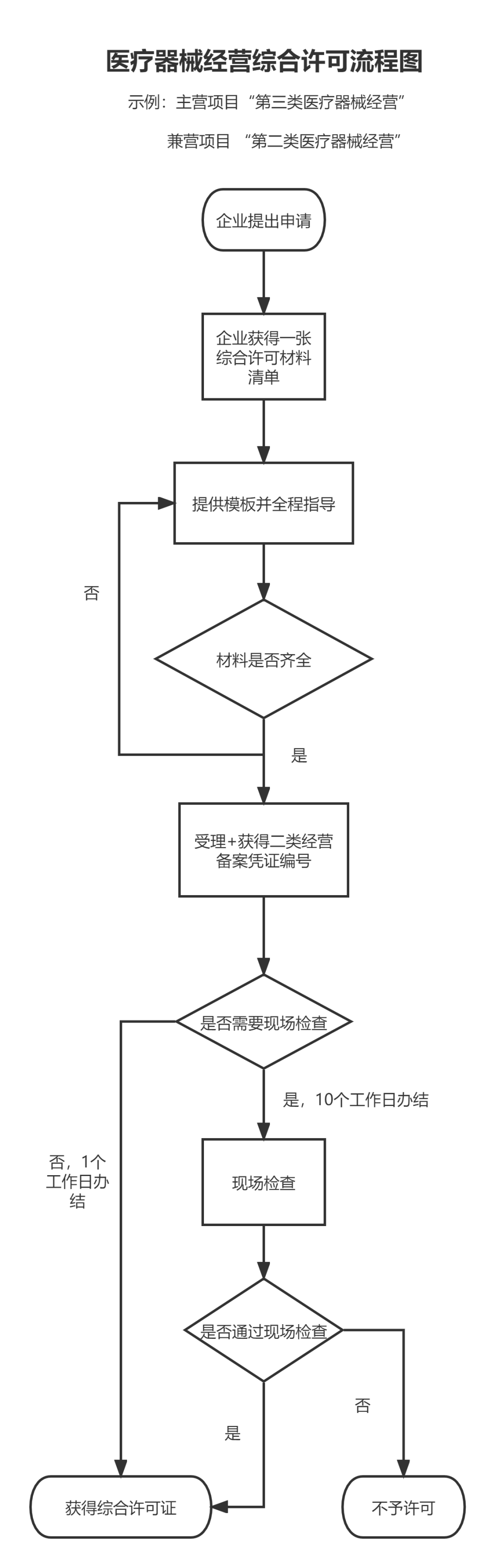
02材料清单库
扫描或者识别以下二维码可以下载材料清单

材料清单库持续更新中......
请先下载《清单目录》,再根据具体情况下载对应的材料清单。
03材料模板
扫描或者识别以下二维码可以下载材料模板

04线上申请流程
以主营项目“第三类医疗器械经营”为示例
在电脑端搜索“河南政务服务网”,点击页面左上角“切换地区/部门”(下图第①步),地区选择“平顶山市”(下图第②步)。
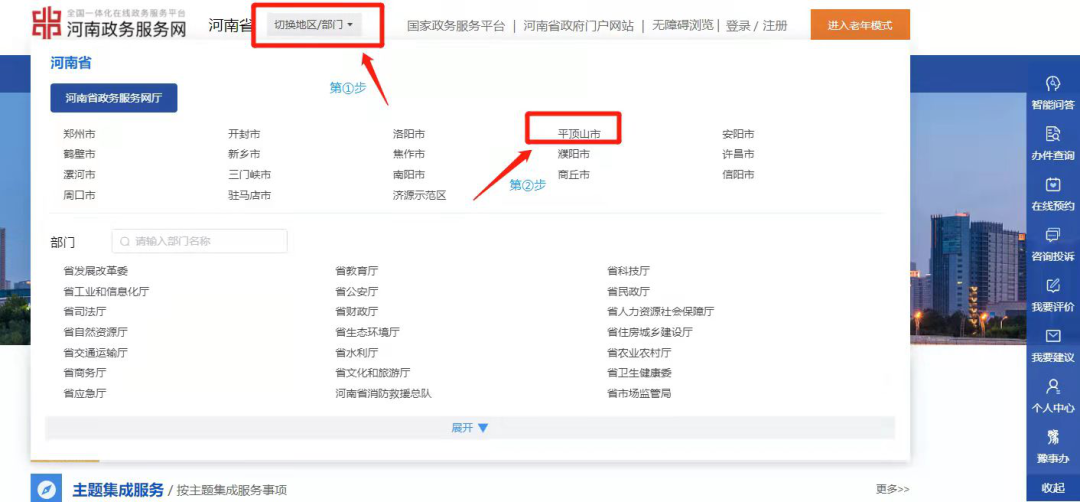
部门选择“市场监督管理局”(下图第③步)。
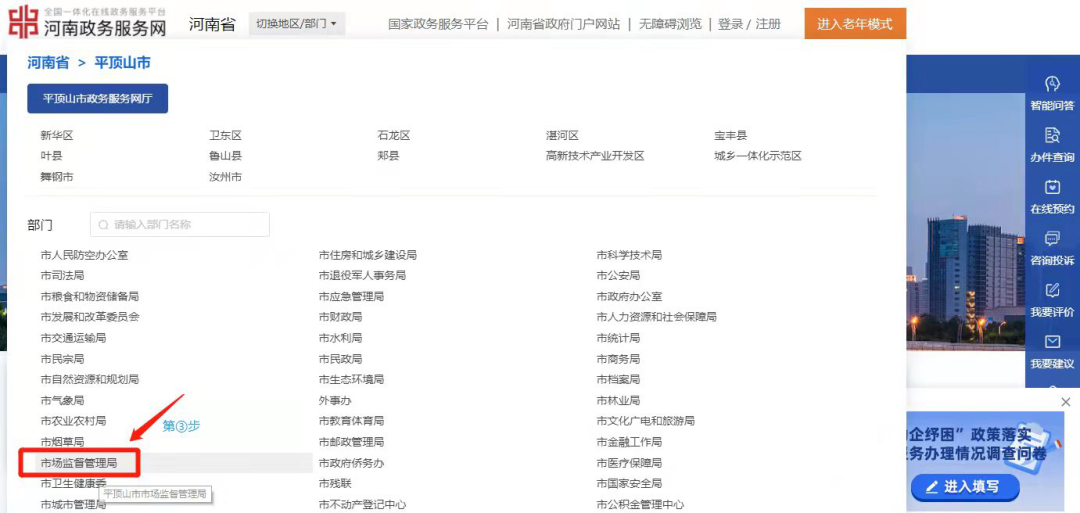
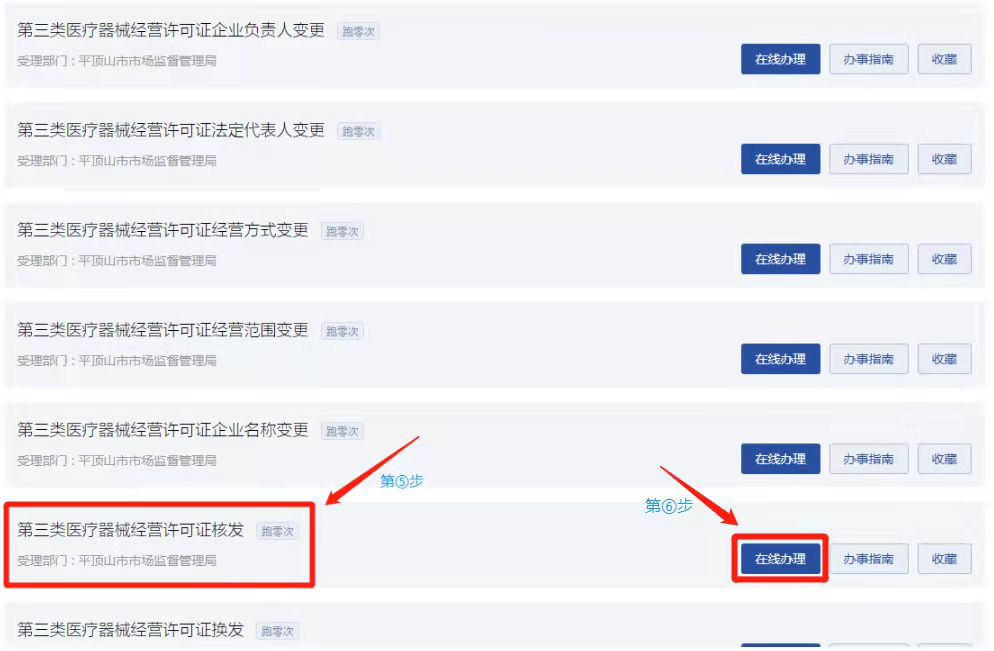
点击选择“第三类医疗器械经营许可”(下图第④步)。
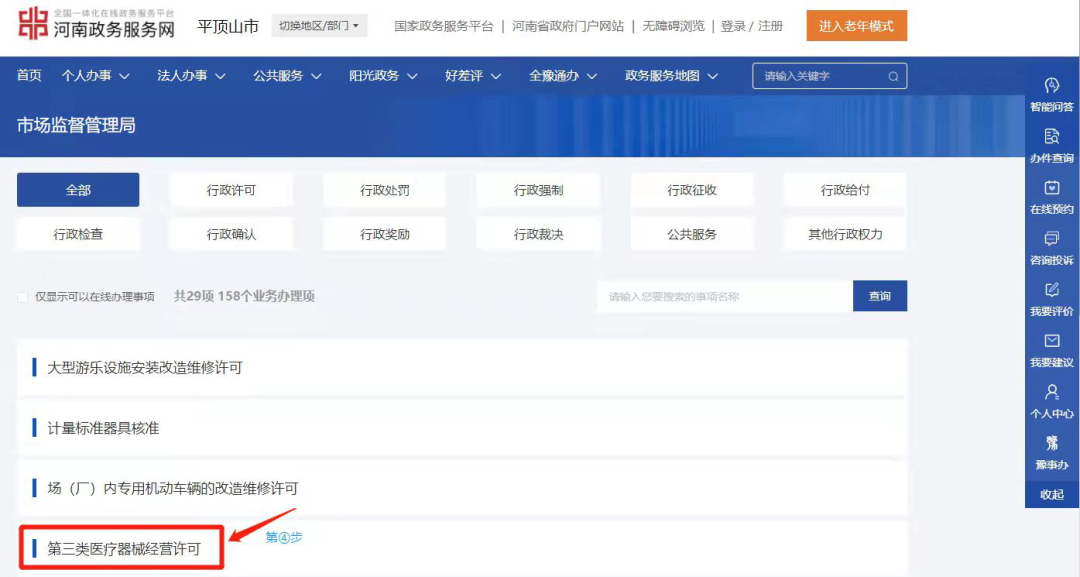
找到业务办理项“第三类医疗器械经营许可证核发”(下图第⑤步),点击“在线办理”(下图第⑥步)进入登录页面。
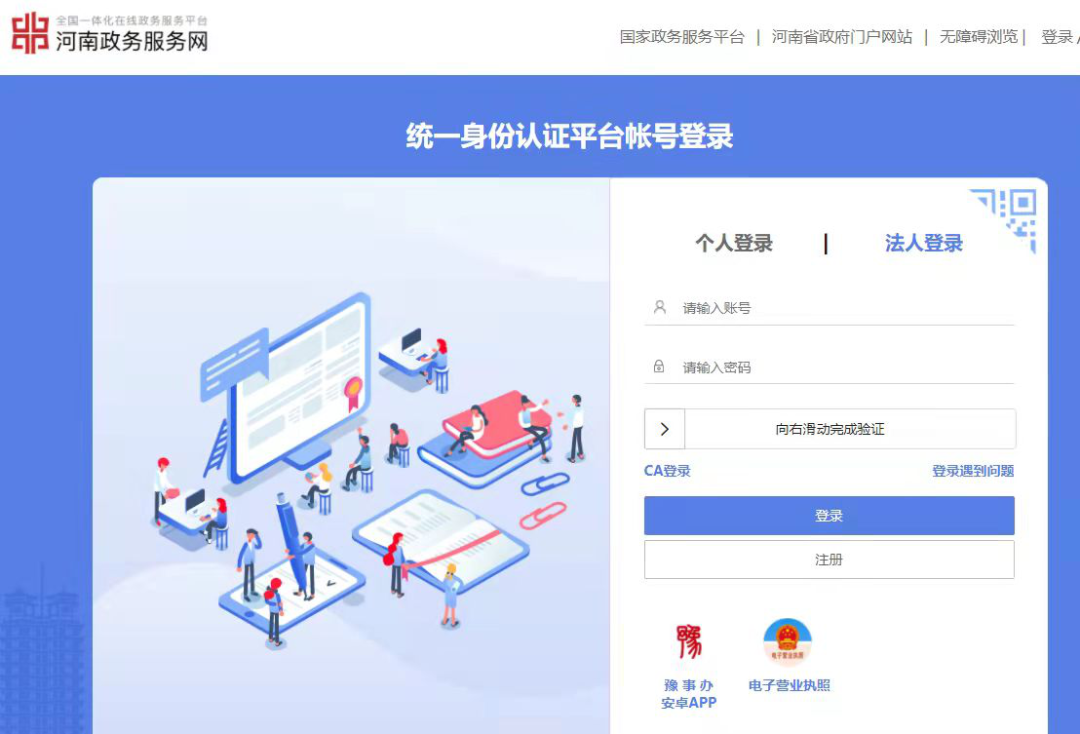
已注册企业,选择“法人登录”。未注册企业,请先注册后再进行登录。
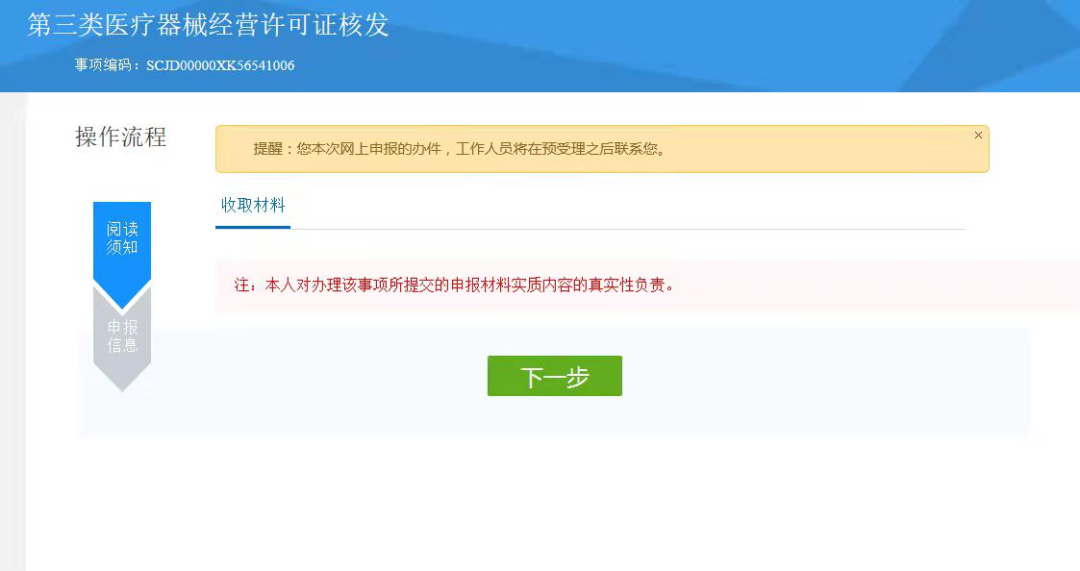
页面进行跳转,点击“下一步”进入操作页面
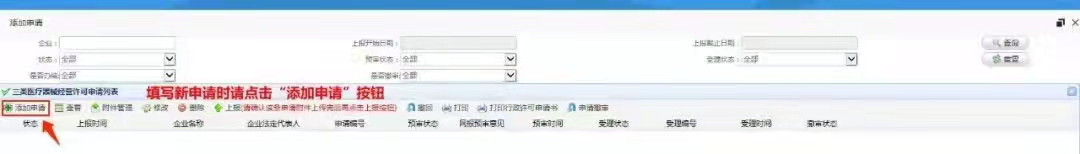
点击“添加申请”按钮,填写新申请
信息填写注意事项
下图红色方框的信息请与营业执照上的信息保持一致(注意:此系统不会识别信息填写是否错误,请务必认真核对、填写正确)
经营方式选“批发”“零售”“批零兼营”其中一个,经营范围需要企业根据自身实际情况选择。
质量管理人员人数:经营方式为“零售”的企业可以写“1”,经营方式为“批发”或者“批零兼营”的企业建议写“3”以上。
拟提交至选择“平顶山市”-“平顶山市本级”
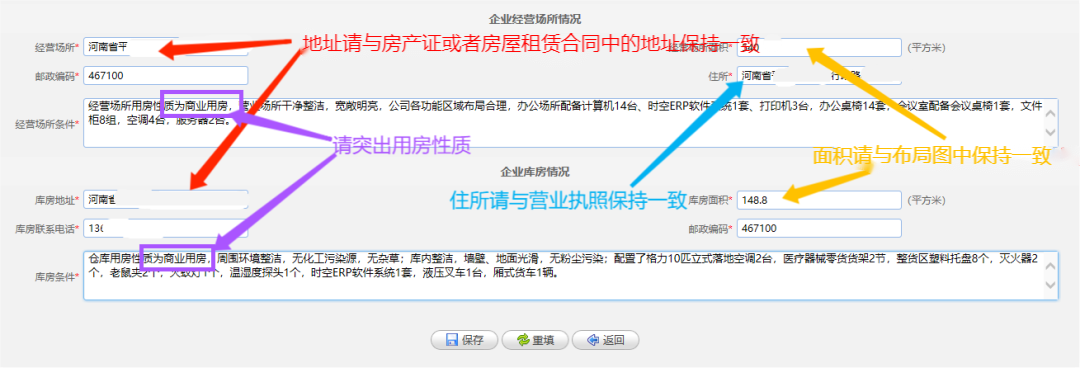
经营场所条件和库房条件
需要突出用房性质;
经营场所面积与库房面积应当与布局图中面积保持一致;
经营场所条件和库房条件中简要写明各自的设施设备情况,并且需要与《经营设施、设备目录》中种类、数量保持一致。
经营范围的选择
原分类目录中“6822-1植入体内或长期接触体内的眼科光学器具”中包含角膜接触镜,如果企业中没有相关专业(眼视光技术专业)或者职业资格的人员(验光员),请不要选择。
注意:经营角膜接触镜的企业的验光人员,需要在组织机构框架图、各部门职能说明、医疗器械从业人员情况表中加以体现。该人员不可在其他企业兼职。)
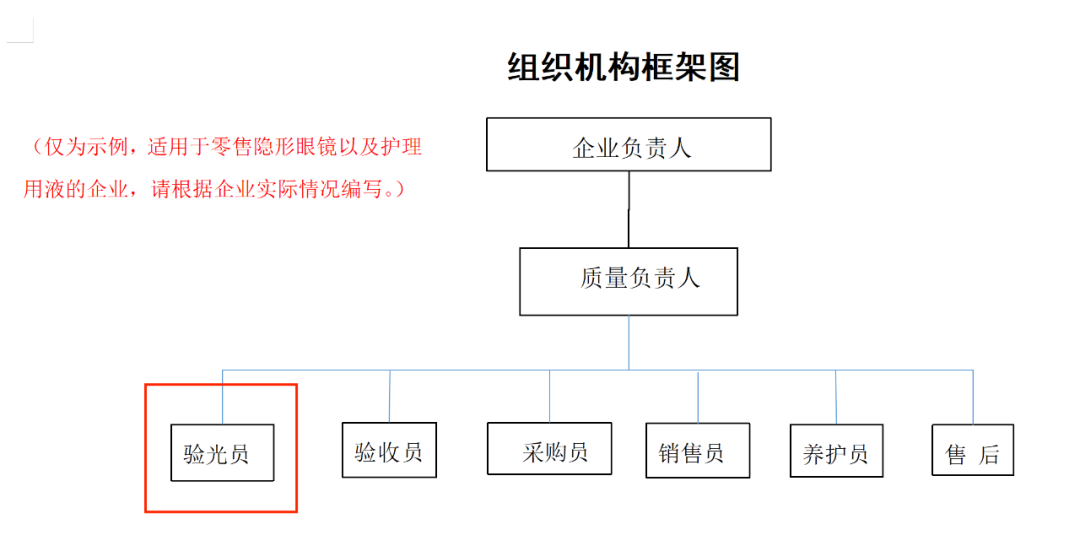
零售隐形眼镜和护理用液的企业经营范围按照下图中的内容填写
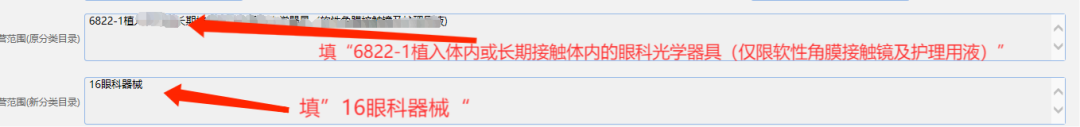
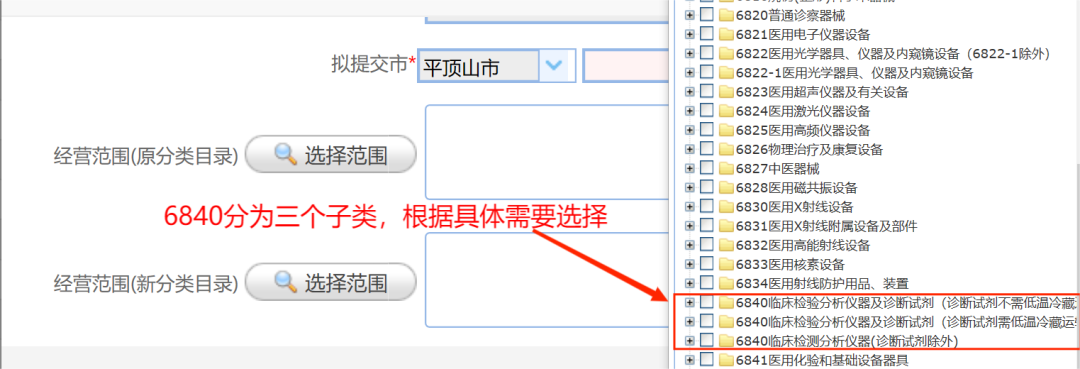
原分类目录中6840临床检验分析仪器在系统中共分成3个子类,“6840临床检验分析仪器及诊断试剂(诊断试剂不需低温冷藏运输贮存)”“6840临床检验分析仪器及诊断试剂(诊断试剂需低温冷藏运输贮存)”“6840临床检测分析仪器(诊断试剂除外)”,企业应当根据实际情况选择。![]()
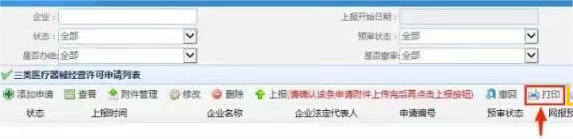
打印申请表
信息填写完整之后,需要打印申请表,如图点击红色箭头所指位置打印。
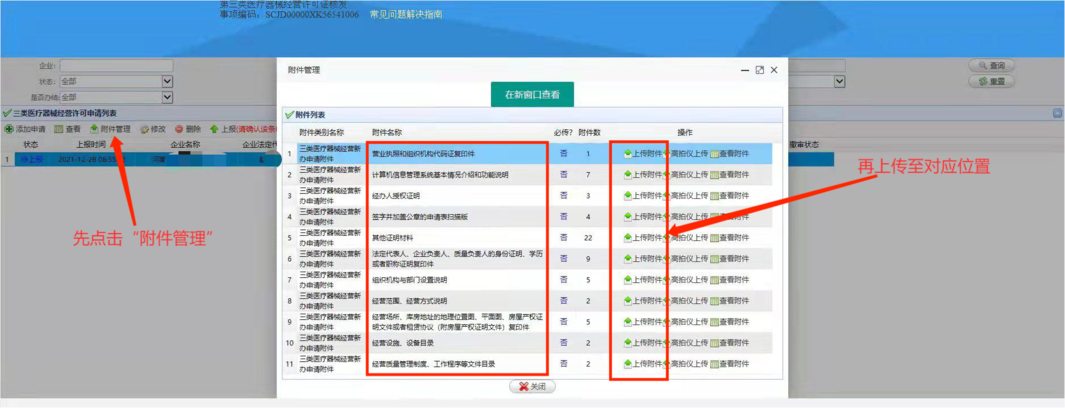
材料清单中所有材料均需要打印、签字、盖章、扫描并上传至线上申请流程的“附件管理”中对应的位置,请务必保证上传完整。
注意:兼营项目的线上申请流程参照第三类医疗器械经营的,受审批系统的限制,目前各个项目需要分别填写线上申请流程。
05材料基本要求
申请材料必须与现场情况相一致。涉及需要签字的,不可以代签字。申请材料需要打印并逐页加盖企业公章。材料中所有的复印件需要保证清晰、完整,且需要法定代表人或者委托代理人签上“经核对 与原件一致”并签名。
06特别注意事项
①房屋
医疗器械经营场所和库房均需要满足“不设在居民住宅内、军事管理区(不含可租赁区)以及其他不适合经营的场所”的条件(以下简称“满足前述条件”)。
如果拟办企业仅有一处房屋可以使用,且该房屋房产证上写明的规划用途是“住宅”,建议一开始就不要用该房屋来申办医疗器械经营企业的营业执照。
如果拟办企业的经营场所和库房不是同一房屋,则两处房屋都需要满足前述条件。
一般情况下,需要提供房屋产权证明文件,如不能提供,则至少需要提供符合要求的房屋租赁协议复印件。
房屋租赁协议中承租方应当是该企业,而不是企业的法定代表人或者负责人。

经营场所和库房的地址应当尽可能详细到门牌号、房间号。
②质量负责人
不得兼职要求:企业负责人与质量负责人不能为同一人,质量负责人不能在其他企业兼职。
专业范围要求:质量负责人应当具备医疗器械相关专业(相关专业指医疗器械、生物医学工程、机械、电子、医学、生物工程、化学、药学、护理学、康复、检验学、计算机、法律、管理等)的学历。
学历/职称要求:大专以上学历或者中级以上专业技术职称。
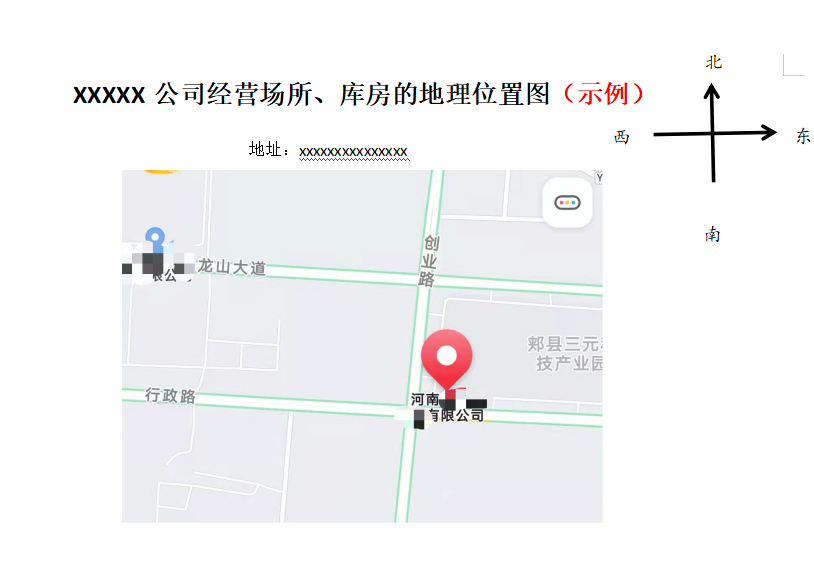
③地理位置图
需要标明地址和方向
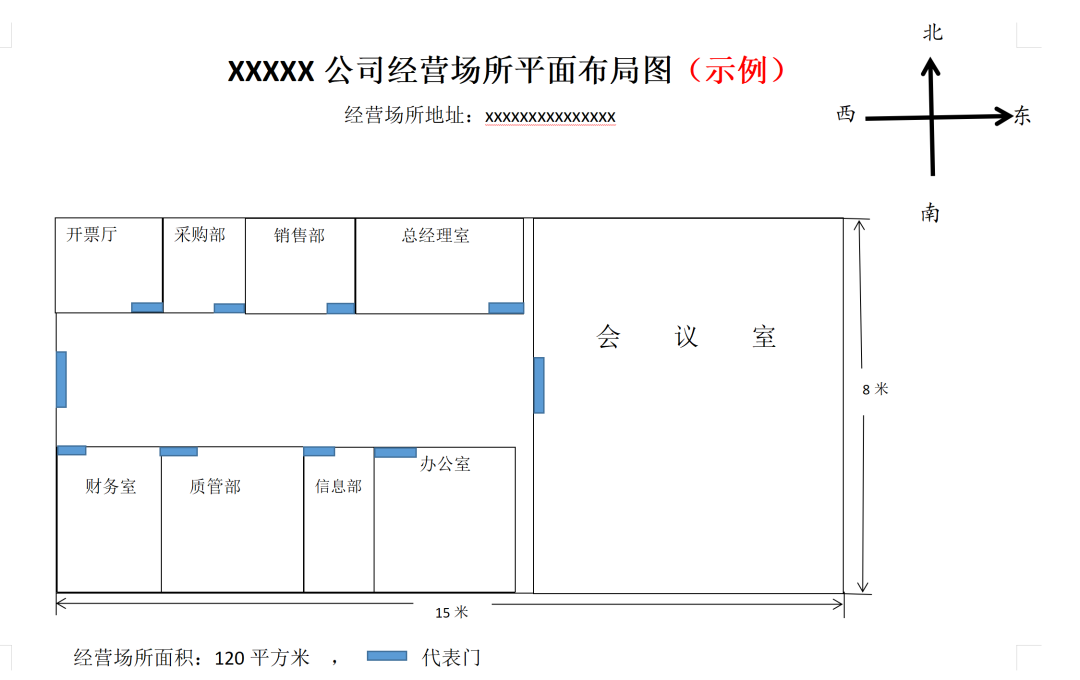
④平面布局图
企业经营场所和库房需要相对独立且经营场所、库房面积需要与其经营范围和经营规模相适应。
经营场所平面布局图
需要标明方向、地址、面积和各个部门
库房平面布局图
库房实行分区管理,包括待验区、合格品区、不合格品区、发货区、退货区等,并有明显区分(可采用色标管理,设置待验区为黄色、合格品区和发货区为绿色、不合格品区为红色),需要标明方向、地址、面积和各分区。
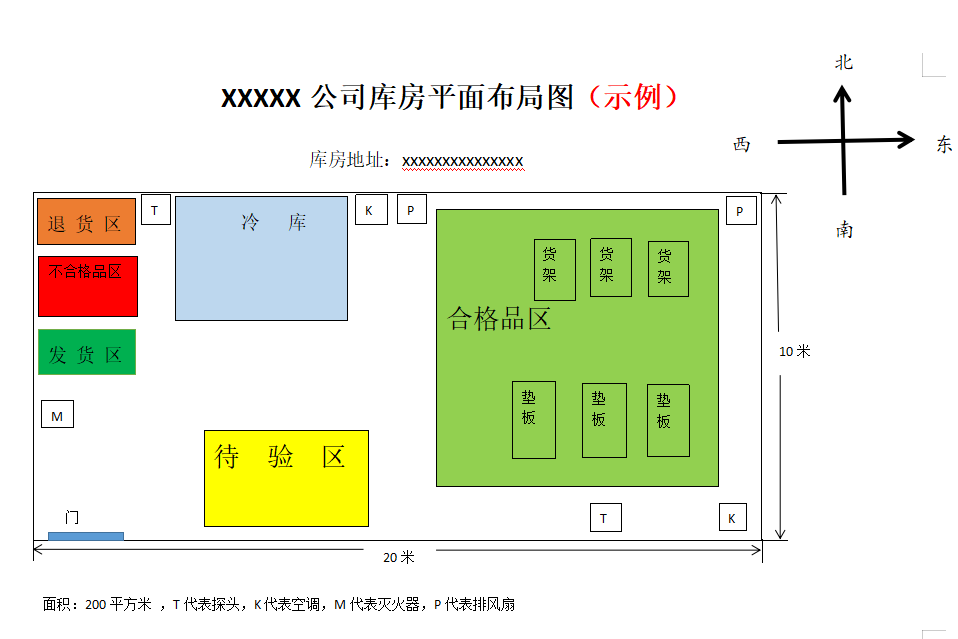
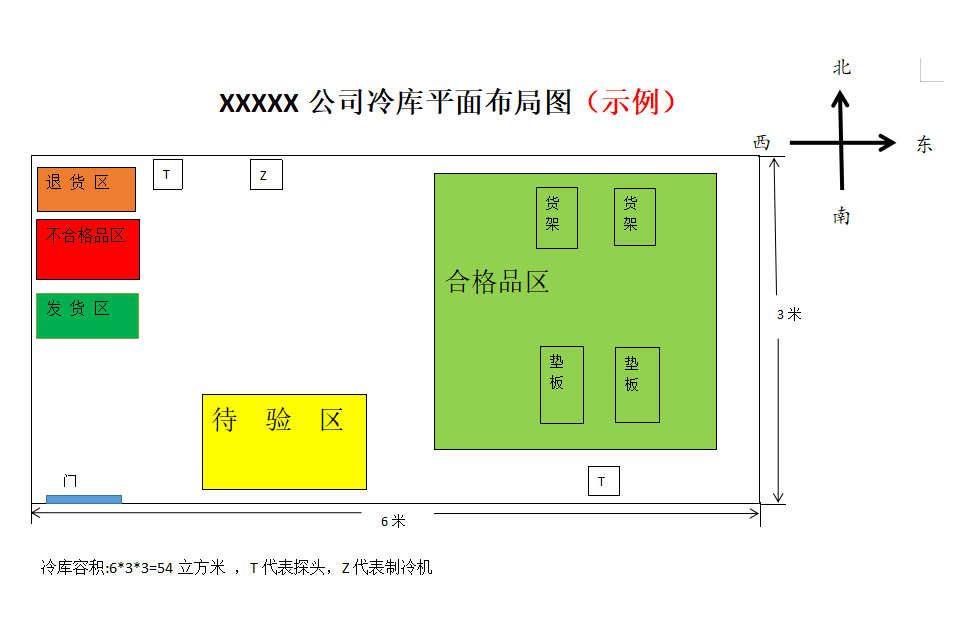
冷库也需要按此要求分区,冷库需要标明容积。
⑤经营设施、设备目录
根据企业实际情况填写,注意计算机信息管理系统也需要写进去,经营需低温冷藏运输贮存诊断试剂的企业需要配置冷库、能确保制冷设备正常运转的设施(如备用发电机组或者双回路供电系统)、冷藏运输设备(冷藏车或者冷藏箱)。

⑥计算机信息管理系统
经营第三类医疗器械的企业,应当具有符合医疗器械经营质量管理要求的计算机信息管理系统,保证经营的产品可追溯。未配备计算机信息管理系统的,现场检查一定不通过。
⑦经营质量管理制度、工作程序
经营质量管理制度、工作程序等文件在提交申请材料时只需提交文件的目录即可,但是现场检查的时候检查组需要查看文件正文。
⑧经营诊断试剂的人员资质要求
经营诊断试剂的企业,应当有1人为主管检验师(检验师中级以上),或具有检验学相关专业大学(本科)以上学历并从事检验相关工作3年以上工作经历。从事体外诊断试剂验收和售后服务工作的人员,应当具有检验学相关专业中专以上学历或者具有检验师初级以上专业技术职称。
END
 豫公网安备 41040202000129号
豫公网安备 41040202000129号